いまさら聞けない基礎用語【ス】#050 水蒸気分圧
公開日時:2025/10/29
みなさん、こんにちは。基礎用語、案内役のあるるです。
今回注目する基礎用語は、コチラ!
↓↓↓
今月の基礎用語:シ #050
水蒸気分圧
(すいじょうきぶんあつ)
water vapor partial pressure (略称は WVPP)
降りそうで降らないどよ〜んと曇った空の下。
かわいい傘をさしたあるるが、なにやら妙な動きを・・・
博士「どうしたのだ、あるる? お、素敵な傘を持っているではないか」
あるる「はいっ! おじいちゃんに買ってもらったおニューの傘なんです。今日こそさせると思って、喜んで外に出てみたんですが・・・」
博士「降りそうで降らないのぅ。今、空の上では水蒸気分圧と飽和水蒸気圧とがせめぎ合っておるのじゃろう。傘の出番はまだなさそうじゃのぅ」
あるる「す、水蒸気はわかりますが、ぶ、分圧? あれ、分圧ってなんでしたっけ? 教えてもらった記憶がうっすら・・・。ちょっとだけ待ってください、今思い出しますから。えっと、えっと・・・」
博士「ふぉっふぉっふぉっ。記憶と忘却が、いい感じにせめぎ合っているのぅ(笑) よし、雨が降る前にちゃっちゃと復習しようぞ」
降りそうで降らない雨は・・・
水蒸気分圧
今回は「水蒸気分圧」のお話です。
まず、空気は色々な気体の混合体であり、それぞれの気体の圧力の総和が大気圧となります。
水蒸気量(g/m3)も水蒸気分圧(hPa)も表していることは同じなのですが、この〝分圧〟という考え方を説明します。
例えば、気温25℃、1気圧で露点温度18℃の湿り空気(水蒸気を含んだ空気)があるとします。
露点温度18℃の飽和水蒸気量は15.4g/m3であり、飽和水蒸気圧は20.6hPaです。
そして、空気の分圧は、標準大気圧1atm=1013.25hPaなので
1013.25-20.6=992.65(hPa)
となります。
複数の圧力を合わせて1気圧というと違和感があると思いますが、分圧というのはこの場合で言うと、
1立方メートル(㎥)の容器に15.4gの水蒸気のみがあった場合、その容器の内圧が20.6hPa になるという事です。
気温が高くなると飽和水蒸気圧(飽和水蒸気量)は高くなり、100℃になると1013.25hPa になります。つまり、水蒸気のみで1気圧になるわけです。
やかんでお湯を沸かしたときに、沸騰して注ぎ口から噴き出している透明の部分が水蒸気です。
水蒸気はすぐに外気で冷却され、飽和水蒸気圧が下がるため、水滴となって水蒸気との混相となったものが湯気であり、水滴となったために目視できるのです。
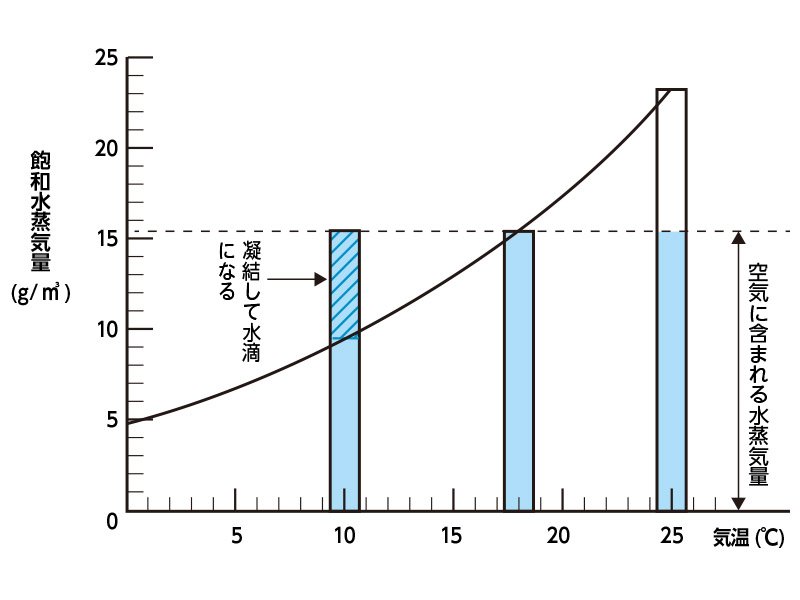
気温と飽和水蒸気量の関係
気液平衡
液体の表面では絶えず蒸発が起こっています。
これは、液体分子が激しく振動しているなかで、他の分子との引力に打ち勝って液面から飛び出すからです。
温度が上がると分子の振動は激しさを増し、蒸発する分子が増加します。
したがって、液体が密封容器に入っている場合、気相の分子の密度が増します。
気体分子の中には液面に衝突して液体内に入るものもありますが、この衝突回数は圧力に比例します。
単位時間内に液体から気体に飛び出す分子と、気体から液体に戻る分子の数が等しいとき、みかけ上、状態の変化は見られなくなります。
この液体と気体が共存している状態を「気液平衡(きえきへいこう)」と言います。
そして、この時の気体の圧力が飽和水蒸気圧です。
飽和蒸気圧が外気圧に等しくなると、蒸発は急激に活発になり、液体の表面からだけではなく内部からも気化が起こります。
これが沸騰であり、気体と液体が共存して温度が一定に保たれ、この時の温度が沸点です。
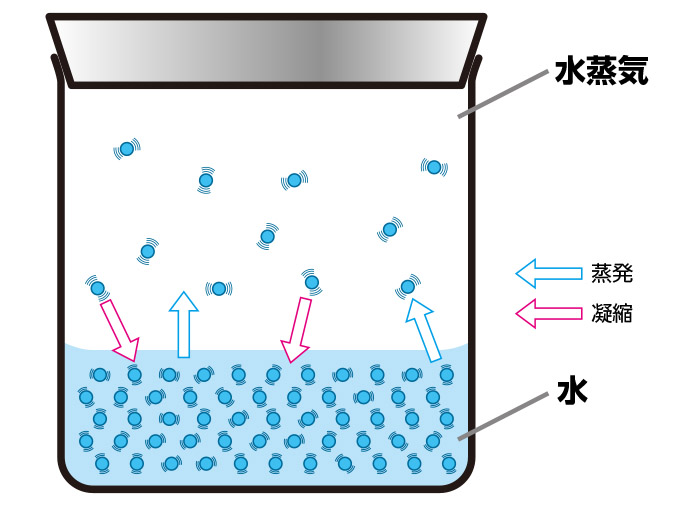
気液平衡:みかけ上、蒸発も凝縮も起っていない状態
あるる「そうでした! 水蒸気と湯気の違い、今ハッキリと思い出しました」
博士「それはよかった。この機会にしっかりと覚えておくのじゃぞ」
あるる「はいっ! そして、あの時食べたスィートポテトの記憶も、鮮明に蘇りました。美味しかったなぁ〜〜」
博士「おじいちゃんの手作りだったのぅ。確かにあれは美味かった。リクエストよろしく」
博士「お、そんなことを言っていたら、雨が降ってきおったぞ。あるる、今がチャンスじゃ!」
あるる「やった〜\(^o^)/ 記念すべき“傘デビュー”してきます。ではっ!(シュタッ!)」
博士「早っ! 元気じゃのう。まるで沸騰して飛び出す分子の勢いじゃ」