【今月のまめ知識 第23回】金属とは何か?
公開日時:2015/02/17
教壇に頬杖をつきながら、珍しくブルーな様子のあるる。
ついているのは頬杖だけでなく、ため息もたくさんついている
そこへ来たアルファ博士。当然のように・・・
博士「どうしたあるる。お腹が痛いのか? それとも腹がすいているのか?」
あるる「違いますよ。ちょっと考えごとをしていただけです」
博士「ほう、珍しいな。雨、いや、雪でも降らんとよいが・・・」
あるる「 博士、前回「アルミはボーキサイトという石が原料」って教えてくれたでしょ。
てことは・・・オリンピックのメダルも、石からできてるってことですよね?」
博士「なんじゃ、突然。今日のあるるはおかしいのぅ。石といっても、その辺に
落ちている石ころじゃないぞ。金属の元になるものが入っている「鉱石」が原料じゃ」
あるる「あれからずっと気になってるんです。なんで石から、あ、鉱石ですよね、
あんなにピカピカした金属ができるのかって・・・」
博士「お、あるるもいよいよ金属に目覚めてきたんじゃな。いい傾向じゃ、うんうん」
博士「しかしな、ピカピカしているだけが金属ではないぞ。
ときにあるるよ、金属というと、他にどんなイメージを持ってる?」
あるる「えっと、硬い、冷たい・・・強いっ!」
博士「強いと来たか。あるるらしいのぅ(笑) よしっ! 今日は
あるるが目覚めたよい機会じゃ。ものすごく基本的な話をするとしよう」
博士「あるるは“金属のそもそも”を考えたことはあるかな?」
あるる「ありませんよ。あるわけないじゃないですかー」
博士「(笑) そりゃそうじゃ。じゃ、一緒に考えてみよう」

みなさんは「金属」というとどんなイメージでしょうか?
「硬いけど割れたりせず、光沢があって、電気を通すもの」で
だいたい合っています。
これまで、アルミフレームや鉄などの金属についてお話してきましたが
そもそも金属とはいったいどのようなものなのでしょう?
今回は金属について、簡単にお話しましょう。
金属の定義
金属とは、冒頭で述べたように
・硬い
・割れない
・光沢がある(ピカピカしている)
・電気を通す
といった特徴を持つ物質の総称です。
化学的に言うと「金属結合するもの」となりますが、
まずは、それはどういうことかを説明しましょう。
自然界に存在する物質は、分子やイオンの集合体で、
分子は原子が集まってできているものです。
原子はどのように結びついているのか? というと、
原子間の結合の仕方の違いによって
・イオン結合(金属元素と非金属元素からなる結合)
・共有結合(非金属元素のみからなる結合)
・金属結合(金属元素と金属元素からなる結合)
などに分けられます。
それではひとつずつ、詳しく解説していきましょう。
イオン結合
「イオン結合」とは、陽イオンと陰イオンが
静電気力(クーロン力)で結びついたものです。
たとえば、金属元素のひとつナトリウム「Na」を
塩素ガス「Cl₂」の中に入れると互いに電子を交換して
ナトリウムイオン「Na⁺」と塩化物イオン「Cl⁻」になり、
これがクーロン力で引き合い、塩化ナトリウム「NaCl」(いわゆる食塩)となります。
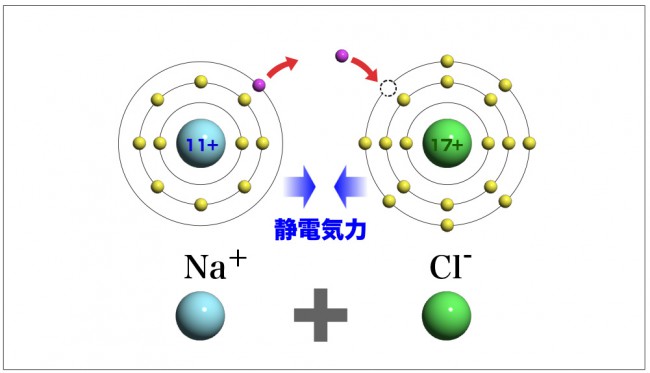
Na⁺ + Cl⁻ ⇒ NaCl(塩化ナトリウム)
共有結合
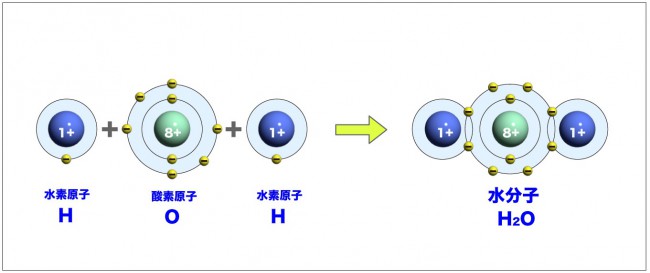
「共有結合」とは、非金属元素の原子核のまわりの価電子
(一番外側の軌道を回っている電子)が隣の別の原子核に引き寄せられ、
互いに交わって、一対の価電子が2個の原子核に共有され
(電子の軌道を2個の原子核が共有している)、より安定した状態となった結合です。
この結合で誕生した原子のグループを「分子」と言います。
例としては、水素(H2)、水(H2O)、酸素(CO2)、二酸化炭素(CO2)などです。
金属結合
そして「金属結合』です。
金属結合とは、金属原子が最外殻を回っている価電子を放出して失い、
陽イオンとなった原子が規則正しく並び、放出された電子が
この陽イオンの中を自由に動き回っている(自由電子と言います)
状態の結合を言います。
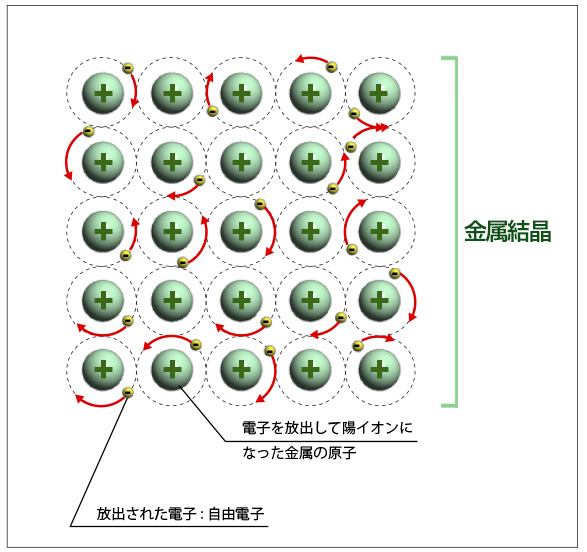
共有結合でも電子を共有していますが、
2つの特定な原子間だけであり
電子が動くことはありません。
一方の金属結合では、規則正しく並んだ陽イオンすべての間を
自由電子が動き回ります。
金属結合により規則正しく配列したものを『金属結晶』と呼び、
以下のような特徴があります。
① 電気伝導、熱伝導が良い
② 一般に融点が高く、展性、延性がある
③ 金属光沢がある
以下に詳細を述べます。
①電気伝導、熱伝導が良い
これは飛び回る自由電子が、電気や熱を伝えるためです。
ですから、電気伝導が良い金属は、熱伝導も良いということになります。
②一般に融点が高く、展性、延性がある
「展性」とは、圧縮する力(打撃など)を与えられて薄く広がる性質のこと。
「延性」とは、引っ張る力を与えられて細く伸びる性質のことです。
共有結合は、原子間の結合が強いのですが
金属結合では結合に寄与する電子を共有しているめ、
原子間の移動が容易で、割れずに変形ができるのです。
結晶の変形は、規則正しく並んだ原子が、結晶面に沿ってすべることでおきます。
この展性と延性があることで、金属は非常に加工性の良い材料として
広く使われているわけです。
③ 金属光沢がある
自由電子はマイナスに帯電しているので、電子同士が近づくと反発し
それを繰り返すために激しく振動します。
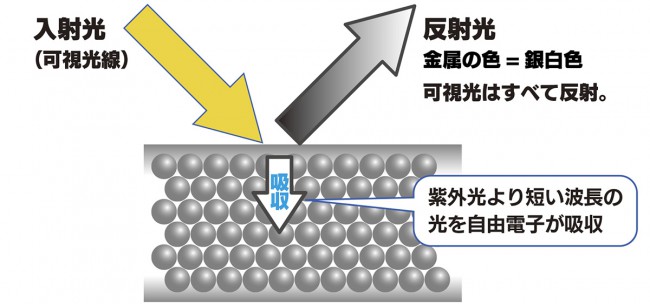
この振動数が可視光の振動数より大きいため可視光は反射され、
金属内部に入っていかず反射が起こり、もとの光と同じ振動数の光を放出するので
光り輝いて見えるのです。
反射する光の波長は金属ごとに異なります。
アルミニウムは可視光線全域の波長をよく反射するので、
銀白色に見えるわけです。
あるる「うわー、アタマがクラクラするぅ〜 (@ω@;)」
博士「居眠りもせず、よく着いて来たな、エラいぞ、あるる」
あるる「電子、結合、結晶・・・♪ でも、こういう基本中の基本の話って面白いんですね。
電子のことなんか、今まで考えたこともなかったですよ」
博士「ふぉっふぉっふぉっ・・・興味を持ってくれてなによりじゃ」
あるる「電子といえば・・・はっ、電子レンジ!!
そういえば考えすぎて、朝から何も食べてませんでした! お昼ご飯、行って来ます!!! =333」

そう言いながら風のように去って行くあるるの姿を眺めながら、
博士「やっぱり、お腹がすいていたんじゃな・・・(遠い目)」